发布时间:2024-05-08 浏览量:0

卵巢早衰不仅会影响生育,还会引起内分泌、皮肤、精神等全身健康问题,卵巢的功能下降会引起性激素水平的降低,进而出现一系列症状,还会增加心血管疾病和性功能障碍的发生风险。
卵巢健康影响女性状态
PART 01
进入青春期后,卵巢逐渐发育成熟。女性生殖系统受雌激素调节,而卵巢是分泌雌激素的主要器官,同时也是生殖系统中最早衰老的器官,更是全身衰老的加速器。
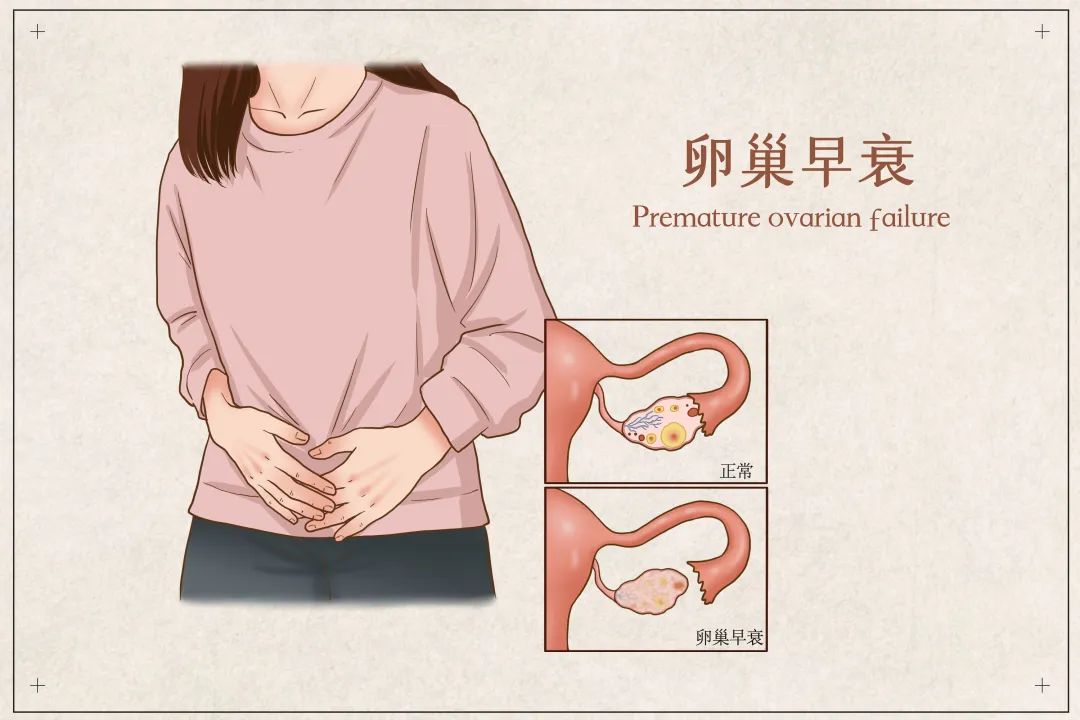
一般情况下,女性朋友在50岁左右卵巢失去正常的功能,进入更年期。医学上来讲,对于未满40岁就失去了卵巢的正常功能,就会被判定为卵巢早衰( Premature ovarian failure,POF)。标准是:40岁以前出现至少4个月以上闭经, 并有2次或促卵泡激素FSH>40IU/L(两次检查间隔1个月以上),雌二醇<73.2pmol/L。
近年来卵巢早衰呈上升和年轻化趋势,卵巢早衰对女性生殖健康的两大威胁主要是雌激素水平降低及影响生育能力,雌激素水平降低增加了女性患骨质疏松和冠心病的危险。
激素替代疗法 (HRT) 是临床上用于缓解雌激素缺乏症状的最常用疗法,但它对生殖功能的影响有限。对于HRT 长期使用也存在争议。
近年来随着对于干细胞研究的深入,越来越多的研究证实,间充质干细胞(MSCs)可以一定程度帮助女性生育力恢复, 助力卵巢“回春”。
干细胞助力早衰卵巢“回春”
PART 02
在2023年6月8日,浙江首例接受干细胞卵巢原位注射治疗后自然受孕至足月的女宝宝健康诞生。接受干细胞治疗六个月之内,患者自然怀孕,且整个怀孕过程也很顺利,于2023年6月8日分顺利分娩六斤多的健康女宝。

这一案例中,该女士在接受干细胞治疗后自然妊娠并成功分娩,与此同时也为临床上卵巢早衰的治疗提供了新的思路。
在一篇最近发表的系统回顾中,作者选取了截至 2023 年 6 月,关于MSC保护卵巢储备免受损伤和衰老的相关112项研究,结果表明:不同类型的MSCs已经过测试,可以改善卵泡的存活和生存质量,还能够逆转化疗引起的卵巢损伤,并通过促进卵巢血管的再生长来改善卵泡池的存活[5]。

大量研究证实了MSC在卵巢衰老模型和卵巢损伤模型中的有益效应。
案例一
改善81.3%参与者的卵巢功能:

项目中,干细胞卵巢移植(ASCOT)2周后窦状卵泡计数有明显改善,提高反应较差患者的生殖潜能。以窦状卵泡计数增加三个或更多卵泡和/或连续两次增加抗卵巢激素水平为成功标准,81.3%的妇女卵巢功能得到改善。
案例二

该项目是国内开展的临床实验,26例因复发性IUA引起的不育症患者参加了这项前瞻性,非对照,I期临床试验,并进行了为期 30 个月的随访。结果未发现与治疗有关的严重不良事件。
术后三个月,患者平均最大子宫内膜厚度增加,宫腔粘连评分较应用前降低。组织学研究显示 ERα(雌激素受体 α),波形蛋白,Ki67和vWF(von Willebrand因子)表达水平上调,而ΔNP63表达水平下调,表明应用后子宫内膜增生,分化和新血管形成得到改善。DNA短串联重复序列(STR)分析显示,再生的子宫内膜仅包含患者 DNA。
截至 30 个月的随访期结束时,这26名患者中有10名已怀孕。
未来展望
PART 03
MSCs针对生殖系统衰老的有效性已经通过多项基础和临床研究得到了初步的证实。一系列临床研究提供了有关间充质干细胞针对卵巢早衰等生殖系统衰老的积极信号。

但干细胞针对于卵巢早衰仍然需要更多的高质量、大规模的临床试验来验证MSCs治疗的安全和有效性,并确定最佳应用方案,我们也期待早日实现更高效的治疗效果,帮助更多的女性走出卵巢早衰的困扰。
【注】文章内容旨在科普细胞知识,进行学术交流分享,了解行业前沿发展动态,不构成任何应用建议。


