发布时间:2024-05-21 浏览量:0

嵌合抗原受体(CAR) T细胞治疗于1989 年由Zelig-Eshhar 首次提出,在血液系统恶性肿瘤治疗中已表现出显著的疗效,截至目前全球已有约10 款CAR-T 产品获批[1]。此外,众多临床试验结果显示,CAR-T 疗法不仅在白血病、淋巴瘤、多发性骨髓瘤等血液肿瘤的治疗中疗效卓越,在卵巢癌、肺癌、胃癌、胰腺癌、结直肠癌等实体肿瘤也具有较大的治疗潜力[2],超过700项CAR-T试验正在积极招募患者,进一步说明了CAR-T细胞疗法的快速发展。
CAR- T疗法已历经五代的发展(见下图),通过对CAR结构的设计创新和优化,已有不少临床前研究显示出良好的疗效和安全性,极大地拓展了CAR-T疗法的临床应用,但在cGMP CAR - T细胞生成过程中,细胞培养的关键参数(如pH或氧合)很少被主动监测。全面了解这些因素在CAR-细胞制备过程中所起的作用可能有助于优化患者特异性CAR - T细胞治疗,从而使患者获得最大的疗效以及最小的毒性。
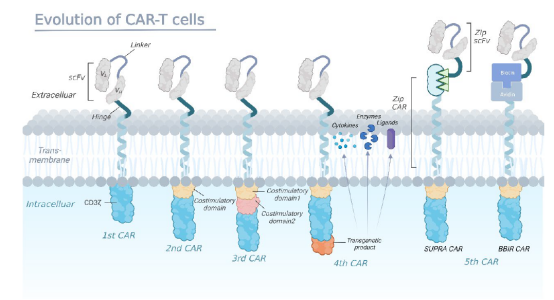
图 | CAR-T的5代发展历程
随着新的CAR - T细胞疗法商业化并进入临床使用,生产稳定的、高质量和高效力的CAR - T细胞至关重要。细胞培养是一个动态的过程,了解细胞、培养基、营养物质和生长因子之间的相互作用对于生产高质量和有效的细胞治疗产品至关重要。在CAR-T细胞制备过程中,常规监测CAR-T细胞活率、表型、CAR 阳性率、无菌检测、支原体、热原/内毒素的检测等指标,很少关注代谢物、氧气和二氧化碳张力或PH等变量。然而这些因素可能与CAR - T细胞增殖和适应性有关。pH值虽然是一个简单的指标,但可以反映二氧化碳张力,乳酸积累和T细胞增殖率。因此,监测这些变量在预测最终细胞治疗产品的特性方面可能有一定的价值。

培养基特性不仅可以作为T细胞扩增的指标,还可以作为潜在的干预点。培养基的pH值已被证明会影响T细胞的增殖、分化和代谢。在酸性培养基(pH 6.6或更低)中培养的T细胞活化、增殖和向抗原特异性细胞毒性T淋巴细胞分化的速度减慢。T细胞在酸性培养基中的扩展引发T细胞代谢重编程,糖酵解受限,长链脂肪酸代谢增加。准确监测和控制pH值和代谢物可能是确保最佳CAR - T细胞性能和功能的重要方式。然而,这些因素在临床GMP CAR - T细胞生成过程中很少被监测,它们对CAR - T细胞生长和分化的影响尚未得到充分研究。
Michaela等人检测了抗CD22 CAR - T细胞培养物的pH和代谢参数,并探讨了培养条件与临床结果之间的关系。纳入研究的产品来自20名被诊断为复发性或难治性表达CD22的B细胞恶性肿瘤的儿童和年轻人,并参加了抗CD22 CAR - T细胞(NCT 02315612)的1/2期临床试验。在细胞培养至第二天时将产品分为低PH组(12个样品 ,PH范围从7.093-7.289;平均值7.2))和高PH组:(8个样品,pH范围为7.323 ~ 7.541;平均值7.4)。Michaela等人的研究显示,CAR - T细胞制备过程中的pH波动与细胞产物的性质相关,并可能指示临床结果。
在细胞生产开始时,低pH值与CAR - T细胞的生长、扩增和代谢活性相关
PART 01
生产开始时的高pH值与有核细胞数量减少、细胞扩增减慢和T细胞代谢重编程有关(图2)。在低和高pH组之间比较了细胞因子和生长因子的水平,与高pH组相比,低pH组的样品中有6种分析物的含量明显更高(图3),低pH组的样品中干细胞因子(SCF, p < 0.04)、巨噬细胞集落刺激因子(M-CSF, p < 0.004)、白血病抑制因子(LIF, p < 0.0052)、白细胞介素15 (IL-15, p < 0.0066)、白细胞介素受体2 α (IL2Rα, p < 0.0002)和肿瘤坏死因子β (TNF-β, p < 0.0001)的水平升高,表明更活跃的T细胞将分泌更多的细胞因子和生长因子到细胞培养基中。从较低pH开始的细胞增加了几种细胞因子的产生,包括IL-6、IL12p70、TNF-a和GM-CSF,这些细胞因子不仅在CAR -T细胞的靶向细胞毒性中发挥重要作用,而且在脱靶效应的发展中发挥重要作用,如CRS和神经毒性。
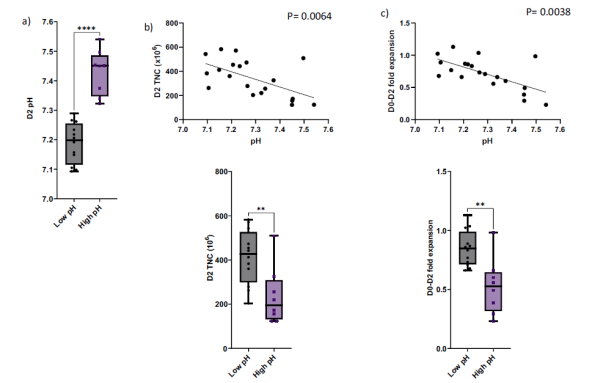
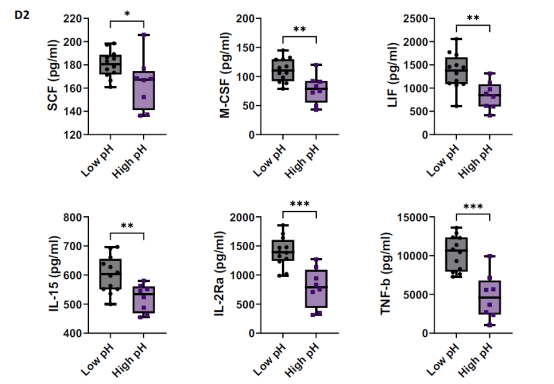
低pH值与临床反应相关
PART 02
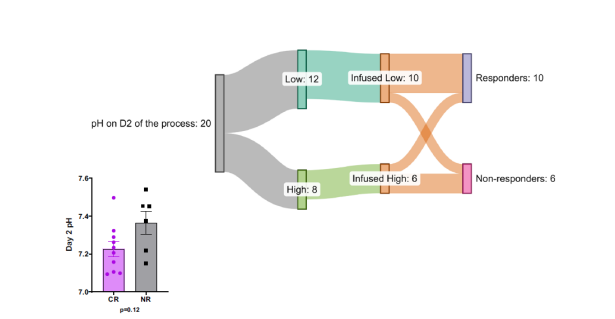
通过分析低pH组和高pH组之间的疾病反应率发现,在D2低pH组的12名患者中,10名患者进行了输注, 在接受细胞治疗的患者中,8例(80%)达到完全缓解(CR),其定义为28天的完全骨髓缓解。高pH组6名患者接受了CAR - T细胞输注。与低pH组相比,在高pH组中,只有2例(33%)患者达到临床缓解,4例(67%)患者没有达到临床缓解。由此可见达到完全缓解的患者多集中在低PH组CR为80%,而PH组CR仅为33%。因此,在生产开始时,细胞pH值较高的患者往往具有较低的临床反应概率(图4)。
▲FDA初次批准CAR-T免疫治疗方法治疗白血病(图源:FDA)
在CAR - T细胞生产过程中,pH值的测量与细胞增殖以及CAR - T细胞的其他代谢特性存在相关性[3],准确的pH跟踪可以作为细胞产品质量的重要指标,并可能成为CAR - T细胞临床疗效的预测指标。在CAR - T细胞生产的整个过程中都需要监测pH,结合其他因素,可以显著提高CAR - T细胞的质量、相容性和安全性。
未来展望
PART 03
随着医学技术的发展,CAR-T细胞免疫疗法越来越多的出现在大众的视野。作为近年来免疫治疗最火热的一种,CAR-T疗法的发展受到整个医学界及学术界的关注。
近期,Nature杂志及其子刊相继发文,阐述了CAR-T免疫细胞治疗的前景。其中一篇发文表示,来自临床和临床前研究的证据强调了CAR - T疗法在肿瘤以外的应用潜力,比如在治疗自身免疫、慢性感染、心脏纤维化、衰老相关疾病和其他疾病方面的潜力。

随着临床的发展,近年来,CAR-T免疫细胞治疗成为了细胞治疗的“主流”,尤其是在针对血液恶性肿瘤方面的成效备受瞩目。从CAR-T疗法到其他的免疫细胞疗法,随着研究的不断深入,相信在未来医学领域中免疫细胞疗法一定会将发挥更加重要的作用,将为人类健康带来更多的福音!


