发布时间:2021-06-23 浏览量:0
2021年6月22日,根据中国国家药品监督管理局药品批准证明文件最新公示显示,由复星凯特生产的CAR-T细胞治疗产品益基利仑赛注射液(又称阿基仑赛,代号:FKC876,受理号CXSS2000006国)已正式获得批准上市,这意味着中国终于等来了CAR-T疗法上市,这也是中国首款获批上市的CAR-T细胞治疗产品,相信紧随其后,中国将全面进入CAR-T细胞疗法新时代。

1、什么是CAR-T疗法?
CAR-T(Chimeric Antigen Receptor T-Cell Immunotherapy)免疫细胞治疗是通过基因工程修饰患者自体T细胞,以表达靶向肿瘤抗原的嵌合抗原受体分子,由激活的T细胞介导杀伤肿瘤细胞。
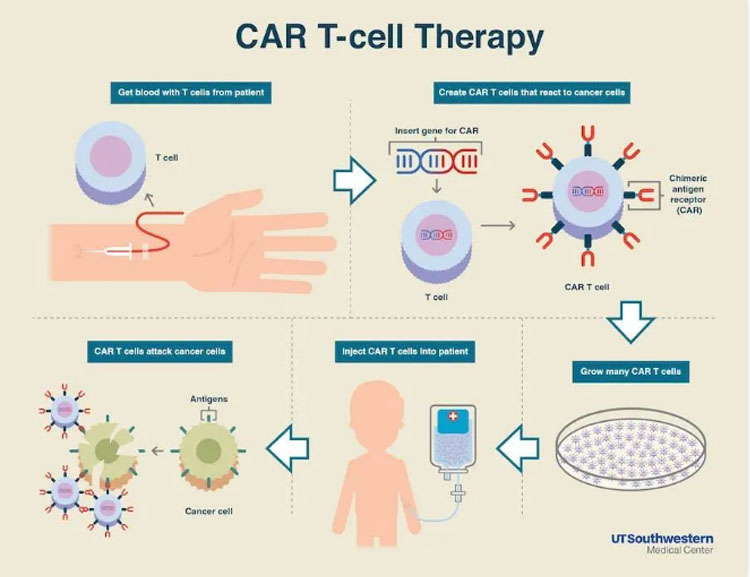
T细胞也叫T淋巴细胞,是人体白细胞的一种,来源于骨髓造血干细胞,在胸腺中成熟,然后移居到人体血液、淋巴和周围组织器官,发挥免疫功能。其作用相当于人体内的“战士”,能够抵御和消灭“敌人”如感染、肿瘤、外来异物等。
CAR-T技术就是把病人的免疫T细胞在实验室通过生物技术改造,将T细胞激活,并装上定位导航装置CAR(肿瘤嵌合抗原受体)再回输体内,这样T细胞这个普通“战士”变身为“超级战士”,即CAR-T细胞,利用其“定位导航装置”CAR,专门识别体内肿瘤细胞,并通过免疫作用释放大量的多种效应因子,它们能高效地杀灭肿瘤细胞,从而达到治疗恶性肿瘤的目的。
2、细胞免疫治疗领域:CAR-T疗法为主流
2017年8月30日,FDA批准诺华公司的CAR-T疗法 Kymriah(CTL-019)上市,用于治疗复发性或难治性儿童、青少年B细胞急性淋巴性白血病。CAR-T这个名词开始广为人知。同年10月18日FDA批准Kite Pharma的CAR-T疗法 Yescarta(KTE-C10)上市,用于治疗复发性或难治性的特定类型成人大B细胞淋巴瘤。因此,2017年也被称之为“CAR-T疗法元年”。
此后,FDA又陆续批准了三款CAR-T细胞疗法上市:
2020年7月
获批的吉利德/Kite的CAR-T疗法Tecartus,用于治疗复发/难治性套细胞淋巴瘤(MCL)成人患者,这是首款获批治疗MCL的CAR-T疗法;
2021年2月
获批的百时美施贵宝(BMS)的CAR-T疗法Breyanzi,用于治疗至少2种其他全身疗法后无应答、或治疗后复发的某些大B细胞淋巴瘤成人患者;
2021年3月
获批的百时美施贵宝/Bluebird共同研发的CAR-T疗法Abecma,用于治疗经过4种或更多种先前疗法(包括免疫调节剂,蛋白酶体抑制剂和抗CD38单克隆抗体)的复发/难治性多发性骨髓瘤患者。这是首个获FDA批准上市的靶向BCMA的CAR-T疗法。
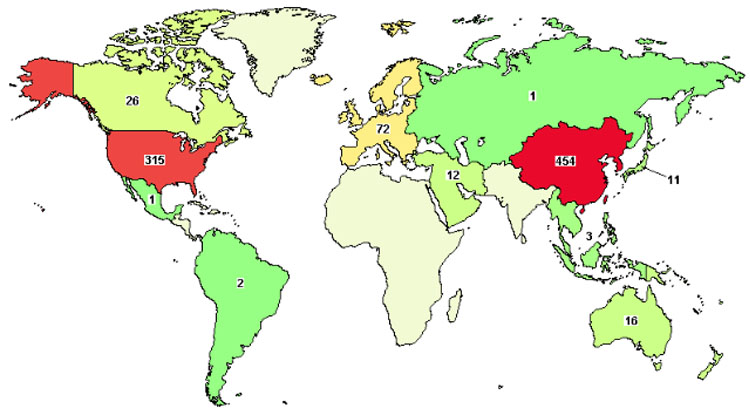
根据世界临床试验中心的数据,目前中国和美国已经成为全球最大的CAR-T细胞疗法的研发国,临床试验项目远高于其他国家。在国内,已有335个正在进行的CAR-T临床试验,其中,多款产品即将步入商业化阶段。且在前期扎堆于CD19靶点之后,国内很多CAR-T细胞疗法已经将眼光瞄准实体瘤,寻找使用CAR-T细胞疗法突破实体瘤治疗的契机。
齐鲁细胞以干细胞和免疫细胞技术为核心支撑,主要开展细胞技术的临床科研与转化服务、CAR-T等免疫细胞产品、拓展成人细胞存储业务、开发新型细胞衍生物系列产品,提供个体化治疗方案。涉及产业上、中、下游的全链条产品研发,是细胞治疗行业为数不多的涉及全产业链的高新技术企业。

其中,公司近年来致力于CD19CAR-T的科研技术突破与临床转化研究,与国内天津、北京及济南等多家三甲医院开展临床项目合作与推进,攻坚创新,积累大量学术理论及临床数据支持,目前开展的CAR-T细胞治疗在急性淋巴细胞白血病临床研究中,整体CR率达90%
此次中国CAR-T细胞疗法的获批上市之后,中国也将会有越来越多的CAR-T细胞疗法获批上市,齐鲁细胞也将不断在血液肿瘤和实体肿瘤上进行进一步的探索,相信伴随着癌症免疫治疗产品不断取得突破,会有更多的患者获得治疗机会,为患者带来更多治疗希望和机会,延长生命周期。