发布时间:2021-05-14 浏览量:0
多发性骨髓瘤-“啃”骨头的血癌
MULTIPLE MYELOMA
多发性骨髓瘤(MM)是仅次于非霍奇金淋巴瘤的第二大血液恶性肿瘤,其肿瘤细胞起源于骨髓中的浆细胞。特征为骨髓浆细胞异常增生,并且大部分伴有单克隆免疫球蛋白或轻链(M蛋白)过度生成,最终导致器官或组织损伤。MM常伴有多发性溶骨性损害、高钙血症、贫血、肾脏损害,因此也有人称这种病为“啃”骨头的血癌。

MM的治疗经历了传统的化疗时期、造血干细胞移植时期、一直到目前的免疫抑制剂(如来那度胺)和蛋白酶体抑制剂(如卡非佐米)等为代表的新药时期,MM患者的生存时期有所延长。即使如此,MM在很大程度上依然是一种难以治愈的疾病,只有大约45%的患者在确诊后能活过5年,许多患者最终会对现有疗法产生耐药,病情还会反复复发。所以到目前为止,MM仍被认为是不可治愈的疾病,对新治疗方法有着迫切需求。
随着生物医学及免疫学的发展,采用嵌合抗原受体(chimericantigenreceptor,CAR)修饰的T细胞的免疫治疗以其惊人的疗效迅速引起极大的关注。伴随着2017年底两款CAR-T细胞疗法的获批上市,这种新兴的治疗方式不仅得到了临床治疗效果的验证,同时也成为癌症前沿治疗领域的必争之地。
靶向BCMA的CAR-T细胞疗法
CELL THERAPY
B细胞成熟抗原(B-cellmaturationantigen,BCMA)正常表达于成熟的B细胞和浆细胞,在MM中也有广泛的表达,而不在人体主要器官的细胞中表达,是一个非常理想的免疫治疗靶点。
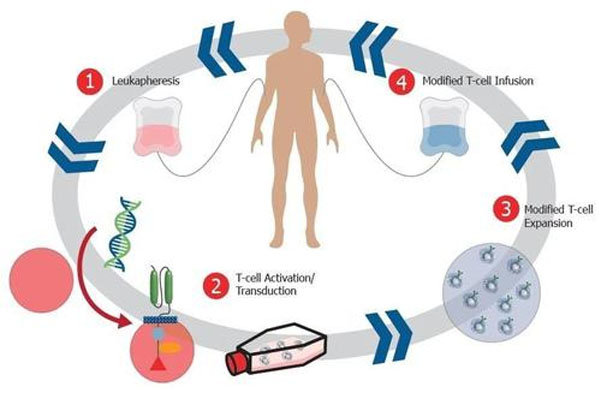
与CD19CAR-T治疗方法的原理相似,BCMACAR-T细胞治疗的原理是在患者的T细胞上嵌合BCMA的受体,从每例患者的血液中分离获得T细胞,使用编码BCMA抗原受体的慢病毒载体对T细胞进行修饰,使T细胞表面表达BCMA受体。治疗时,MM患者先接受化疗药物预处理,以清除患者体内现有的免疫细胞为CAR-T细胞留出生存和增殖的空间,随后输注BCMACAR-T细胞,一旦输注回患者体内,BCMACAR-T就开始寻找并杀死表达BCMA的细胞。
2015年12月
美国NCI的JamesN.Kochenderfer,MD在美国血液病年会报道,利用anti-BCMA-CD28-CD3zeta载体构建的CAR-T细胞,开展了12例患者的临床试验,其中,2例完全缓解(CR),1例部分反应(VGPR),1例部分缓解(PR),5例SD;
2016年12月
Bluebirdbio(蓝鸟公司)公布了其针对治疗复发/难治性多发性骨髓瘤的bb2121的临床1期试验中期数据,显示了这个以BCMA为靶点的CAR-T疗法新产品的良好应用前景。在整个临床试验中,没有出现剂量限制性毒性,患者经历1级和2级细胞因子释放综合征和1级神经毒性。11例患者,不同的剂量梯度中,6个患者有响应,其中2例CR,1例VGPR,3例PR;
2018年12月
美国血液学会(ASH)上,南京传奇和合作伙伴杨森提供了LEGEND-2(NCT03090659)I/II期开放标签研究的最新结果。57名晚期R/R多发性骨髓瘤患者接受了LCAR-B38MCAR-T细胞治疗,ORR为88%。其中,74%的患者达到CR,4%的患者达到非常好的VGPR,11%的患者达到部分反应PR;
2019年
NoopurRaje等报道了其针对治疗复发/难治性多发性骨髓瘤的bb2121的临床1期试验数据,ORR为85%,包括15例(45%)CR。
目前已获批上市的BCMACAR-T疗法
BMACAR-TTHERAPY
2021年3月27日,全球首款以BCMA为靶点的CAR-T细胞经由美国FDA批准用于治疗接受过四种以上前期疗法的复发/难治性多发性骨髓瘤(r/rMM)成年患者。此款新的CAR-T细胞疗法由百时美施贵宝(BMS)和bluebirdbio(蓝鸟)联合开发,其产品名称为Abecma(idecabtagenevicleucel;ide-cel)。
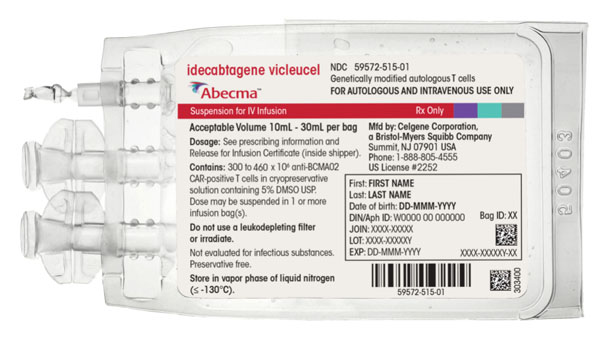
ide-cel获批主要基于关键II期临床试验的结果。该研究中,127例先前接受过至少3种疗法且对最后一种疗法无效的过度预治疗复发和难治性多发性骨髓瘤患者接受了ide-cel剂量水平为300-460x10E6CAR+T细胞治疗。
在接受治疗后可评估疗效的患者中,所有剂量水平的总缓解率(ORR)为72%,其中28%的患者获得完全缓解(CR)或严格缓解(sCR)。治疗后起效的中位时间是30天,中位缓解持续时间(DoR)达11个月,有CR或sCR的患者中位DOR为19.0个月。
与CD19CAR-T细胞疗法的副作用相似,BCMACAR-T细胞疗法也会出现两种副作用—细胞因子释放综合征(CRS)和神经毒性,此产品的整体安全性良好,CRS的3级及以上不良反应的发生率为9%,神经毒性的3级及以上不良反应的发生率为4%。
齐鲁细胞BCMA CAR-T项目研发
RESEARC AND DEVELOPMENT
本公司致力于CAR-T领域的研发,尤其是靶向CD19的CAR-T细胞,在临床研究中达到了很好的治疗效果,当然对于当前热门的BCMACAR-T的研发也是早有布局。从质粒生产、慢病毒载体制备、CAR-T细胞制备、质量研究等均为自主研发。

目前本公司已与医院合作开展BCMA CAR-T疗法的临床研究,随访期内患者全部处于完全缓解期,虽然有一定的副作用,但都在可控范围。相信随着技术的进步和时间的推移,CAR-T疗法会给患者带来更好的治疗效果。