发布时间:2025-04-28 浏览量:0
前言
INTRODUCTION
2025 年 4 月,由国内多位神经内科领域专家共同撰写的《嵌合抗原受体 T 细胞治疗难治性神经系统自身免疫性疾病专家共识(2025 年版)》在《中华神经科杂志》正式发布。此共识的发布,为我国神经系统自身免疫性疾病(NADs)的临床应用提供了全新的规范化指导。

共识指出,目前广泛应用于临床试验并具有初步疗效和安全性的 CAR-T 细胞治疗产品多靶向 CD19 和(或)BCMA 等 B 细胞靶点,因此主要适用于 B 细胞介导或深度参与的难治性 NADs,如视神经脊髓炎谱系疾病、僵人综合征、多发性硬化、Lambert-Eaton 肌无力综合征、重症肌无力、特发性炎性肌病等,并详细阐述了不同 CAR 细胞类型及不同治疗靶点的特点。
同时,共识还提出了 CAR-T 细胞回输后分阶段重点监测方案,提出在不同时间段(如淋巴细胞清除期、回输后 2 周内、回输后 3 个月内及长期监测随访阶段)动态追踪的策略,并针对治疗相关不良反应的处理、复发后处理等,提出了详细的分级管理方案,强调了多学科协作的重要性。
嵌合抗原受体T细胞(CAR-T)疗法是一种治疗肿瘤的新型精准免疫疗法,近年来CAR-T技术通过不断改良优化,在临床中应用取得了很好的效果。
12月12日,《科学》杂志公布了2024年度十大科学突破,CAR-T免疫细胞在自身免疫性疾病中的应用成功入围。“Science年度十大科学突破"是由《科学》杂志每年组织评选的一项活动,旨在表彰一年中全球范围内最引人注目的科学研究成果。

与传统疗法相比,CAR 的内在特异性是其的天然优势,单个 CAR-T细胞还可以呈指数级扩增并杀死数百甚至数千个肿瘤靶细胞。目前,随着CAR组件的不断改进优化,有关CAR-T疗法的临床研究越来越多。
CAR-T细胞治疗在过去的10年取得了惊人的成果,已经有多款CAR-T产品在国内外上市,目前已经上市的CAR-T细胞产品集中在CD19和BCMA 2个靶点,适应症也集中在血液肿瘤领域。另外还有多个靶点的多个血液肿瘤领域的适应症正在开发当中。
如果把CAR-T细胞比作一把利刃,那么利刃出鞘,抵达战场是战争胜利的重要保障。在CAR-T治疗血液肿瘤的过程中,CAR-T细胞在骨髓的浸润是影响CAR-T治疗效果的关键因素之一。目前的研究表明,CAR-T细胞本身表型和骨髓的肿瘤微环境是影响CAR-T细胞骨髓浸润的主要因素。
CAR-T细胞的表型
1)记忆性T细胞表型特征
记忆性T细胞分为中央记忆性T细胞(Tcm)和效应记忆性T细胞(Tem)。人体Tem和Tcm的区分主要依据两点:否产生速发性效应功能:是否表达归巢受体,从而决定这些记忆细胞是迁移到次级淋巴器官还是迁移到非淋巴组织。
中央型记忆细胞( central memory cells,Tcm)为表达CD45RO、CCR7和CD62L。后者使其能够穿越HEV,迁入次级淋巴器官的T细胞区。值得注点的是,初始T细胞也表达CCR7和CD62L.但与之相比Tcm对抗原的刺激更为敬感,较少依赖协同刺激,并可协助上调CD4OL的表达。通过对其TCR的激发,Tcm主要产生1-2,并能迅速分裂,补充周围器官中的效应T细胞。此类细胞主要归至淋巴结,其功能为接受抗原再次刺激后能快速产生效应并上调CD4OL表达:并且能高分泌L-2,并多次増殖,进一步分化为效应性细胞,可长时间维持免疫记忆。
效应性记忆T细胞( effector memory T cell,Tem)主要迁移至外周组织,受抗原刺激后立即产生兔疫效应,发挥细胞毒作用并分泌效应分子。但分泌IL-2及增值能力低下、因比Tem维持免変记忆时间较、主要在免疫防御的第一线发挥作用。
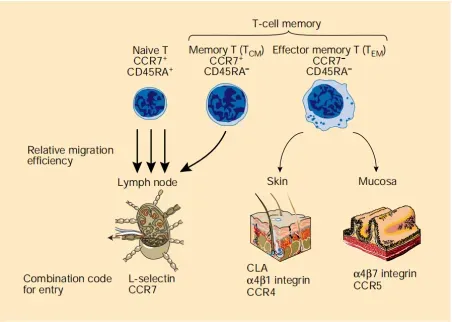
△Nature 401, 659–660; 1999.Dual personality o-
f memory T cells
2)记忆性T细胞在CAR-T治疗中的作用
Martin Stach等构建了CLL的体外模型,选择CLL模型的原因除了肿瘤组织比较容易获取之外,主要是因为和B-ALL相比,CLL对于CAR19的耐药性更强。
最近的研究表明,CLL细胞可以直接抑制CAR19T的增殖和效应功能,并启动CAR T细胞的凋亡。在此研究中,作者发现过表达IL-21可以更好的维持CAR-T细胞的Tcm表型,而Tcm表型有利于CAR-T细胞浸润入骨髓,促进CAR-T细胞的增值和杀伤功能。
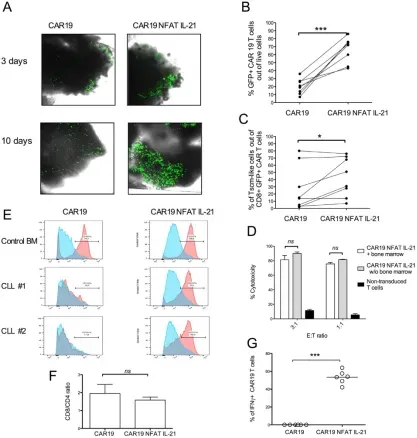
△Cytotherapy, 2020.Inducible secretion of IL-21 augments anti-tumor activity of piggyBac-manu-factured chimeric antigen receptor T cells.
CAR-T细胞表面CXCR4表达在CAR-T治疗中的作用
CXCR4趋化性受体对于造血和免疫细胞的骨髓归巢具有独特的重要性。WHIM综合征患者的CXCR4基因GOF突变会导致NK细胞在骨髓中的良好归巢。转染NK细胞过表达CXCR4或使用CXCR4 GOF突变体可用于白血病的过继细胞治疗。已经探索了其他类似的方法来改善CAR-T细胞向肿瘤微环境的运输,包括强制表达其他趋化因子,包括CCR4、CCR2b、CSF-1R,促进CAR-T细胞浸润入实体瘤。
有报道表明(如下图所示)mTORC1上调和随后的CXCR4下调对CAR-T细胞增值的不利影响,从而损害CAR-T细胞的骨髓迁移及靶向CD33 CAR-T细胞的AML抗肿瘤活性。随后,他们证明了用mTOR抑制剂进行简单的离体预处理可能逆转这种表型的能力。
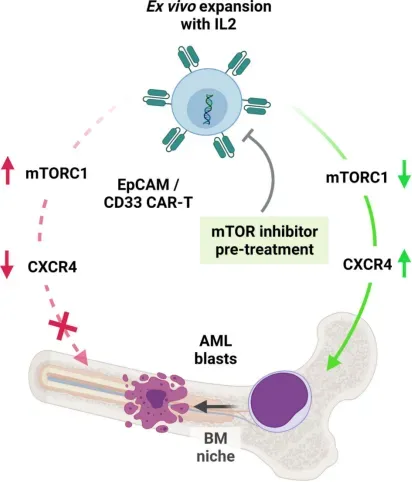
△Clin Cancer Res . 2021.Lowering mTORC1 Drives CAR-Ts Home in Acute Myeloid Leukemia.
CAR-T技术是一种应对肿瘤的新型精准免疫疗法,近年来,CAR-T技术通过不断改良优化,在临床肿瘤临床中应用取得了很好的效果。一些早期结果表明,CAR-T疗法的下一个进展可能是在癌症以外的领域,在其他疾病(如SLE、动脉粥样硬化、肝炎、结核等等)中CAR-T疗法有着不凡的表现。

此次发布的共识,由国内多家知名医疗机构的专家,经过多次研讨和论证,该共识为未来相关临床研究和技术创新奠定了坚实基础。随着研究的不断深入和技术的不断进步,相信未来会有更多有需要的朋友受益于这一技术,重获健康与希望。
【注】文章内容旨在科普细胞知识,进行学术交流分享,了解行业前沿发展动态,不构成任何应用建议。

