发布时间:2024-12-13 浏览量:0

中国慢性病前瞻性研究项目曾公布数据显示,我国冬季心血管患者死亡人数比夏天高41%。一项研究也发现,秋冬季节心血管疾病的发病率占全年的80%,气温每降低1℃,心脏疾病发病率增加2%。
冬季为何被称为心血管病“魔鬼季节”
PART 01
寒冷低温
冬季的低温会导致血管收缩,血管遇冷容易收缩、痉挛,导致心脑血管供血不足,进一步诱发心肌梗死或者脑梗死等意外疾病
干燥
冬季的空气通常较干燥,水分流失引发血液黏稠度增高,增加了心脑血管事件的风险。
高热量饮食
天气寒冷,人们会不自主地过多摄入高热量的食物,胆固醇增高会进一步加重血管动脉粥样硬化,心脑血管疾病的发病率会进一步增高
情绪易波动
冬季日照减少,让人更容易情绪波动,焦虑、抑郁等负面情绪是新发心血管疾病的危险因素,研究表明,抑郁症评分每提高一个标准差,冠心病、卒中和复合心血管疾病的风险比约为1.1。
心血管疾病的现状
PART 02
据《中国心血管健康与疾病报告2023概要》显示,我国心血管疾病现患人数3.3亿,已逐渐升至为威胁人类健康的“第一杀手”。

现有的应对心脏病治疗主要有外科手术,介入治疗及药物治疗。其中药物治疗疗效需要加强,外科手术时造成创面较大,容易诱发各种并发症。相比较而言,介入治疗是一种微创手术,但是同时伴有不同程度的并发症,上述方法均不能起到治疗已坏死心肌的效果。
干细胞具有自我更新和多向分化的能力,可以在体内分化为多种功能细胞,从而修复受损组织。作为再生医学的重要分支,干细胞技术近年来在心血管疾病方向展现了巨大的潜力,在众多干细胞种类中,间充质干细胞(MSCs)成为研究的重点,它来源广泛,如骨髓、脂肪组织、脐带等,且具备免疫调节能力和多向分化潜能。多种优点以及在临床研究中的亮眼表现,为应对心血管疾病提供了全新的思路。
案例分享:干细胞守护心血管健康
PART 03
案例一
2023年,《美国心脏病学会杂志》发布了迄今最大的心力衰竭患者的细胞治疗试验结果。

该研究通过提高心脏泵血能力和降低心脏病发作或中风风险使因射血分数低导致的慢性心衰患者受益。在平均30个月的随访中将心脏病发作或中风的发生率降低了58%,而在具有高水平炎症血液标志物的患者中,益处上升到75%。
这项研究表明:间充质前体细胞(MPC)的特殊免疫调节细胞具有解决心力衰竭的潜力。同时预示着细胞疗法(间充质干细胞疗法)可以一定程度改善患者心力衰竭预后,并且有望和已有的对抗心力衰竭的药物联合使用,发挥协同和附加作用。
案例二
在一项MSCs移植对大鼠快速右心室起搏的心力衰竭治疗实验中,MSCs移植3周后,治疗组的心功能都较移植前有明显改善,室壁厚度增加、心室腔减小、搏动增强;而对照组的心功能、室壁厚度、心室腔无明显变化。由此看出,MSCs可以改善心肌组织的供血和促进心肌细胞再生,对心力衰竭的改善效果明显。
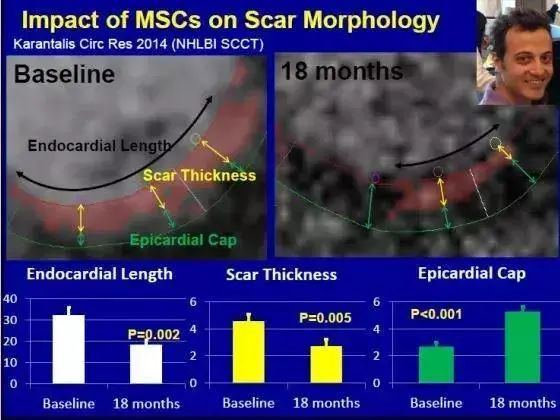
在评估MSCs应对慢性收缩性心力衰竭的有效性研究中,将59例心力衰竭患者随机分为治疗组(n=30)和对照组(n=29)。治疗组接受药物治疗以及脐带间充质干细胞的冠状动脉内移植,对照组仅接受药物治疗。1个月后,治疗组的NT-proBNP和LVEF水平以及死亡率均低于对照组,说明使用MSCs治疗充血性心力衰竭有助于改善心脏重塑功能,降低死亡率,证实了MSCs治疗心力衰竭的有效性。
现阶段,虽然科研人员对于MSCs的实验及临床应用研究已取得了很大的进展,但该领域的研究尚处于探索阶段,但仍有很多问题需要解决 ,但是相信随着对MSCs研究的不断深入及其应用于心血管疾病后令人欣喜的结果,都预示着MSCs广阔前景,但同时还面临着许多问题需要解决。随着人们对MSCs研究的进一步深入,MSCs在心血管疾病中的应用必将拥有更好的未来。
【注】文章内容旨在科普细胞知识,进行学术交流分享,了解行业前沿发展动态,不构成任何应用建议。


